Château Eğitim > Blog > Genel > FRANSIZCA KİMYA – 9ème CLASSE CHIMIE – LIAISONS COVALENTES ET IONIQUES
La liaison covalente est un type de liaison chimique qui unit deux atomes au sein d’une molécule. Elle se forme lorsque les atomes mettent en commun une ou plusieurs paires d’électrons. Ainsi, chaque atome partage des électrons de sa couche externe avec un autre atome afin d’atteindre une configuration plus stable.
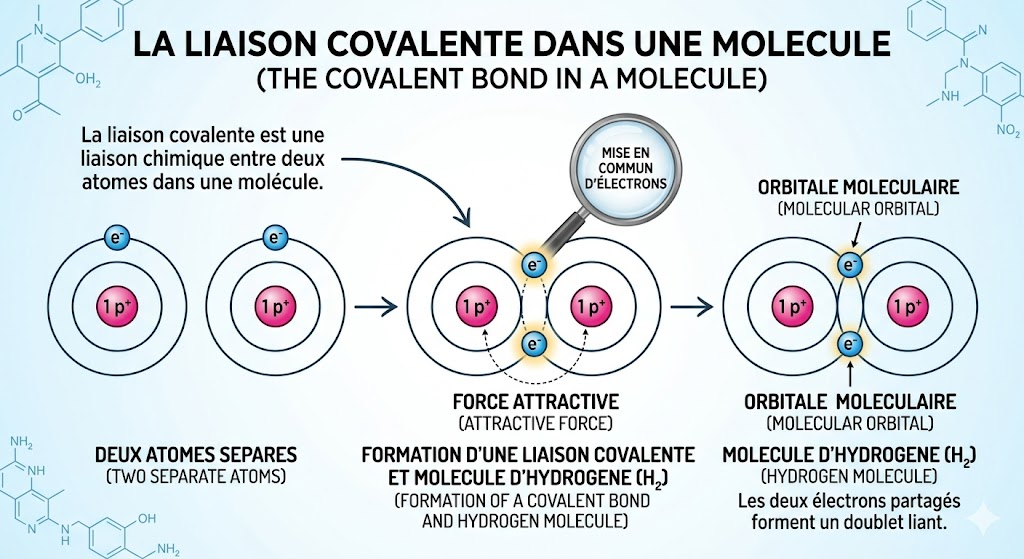
Selon le nombre d’électrons partagés entre les atomes :
- Si une seule paire d’électrons est partagée, la liaison est simple.
- Si deux paires d’électrons sont partagées, la liaison est double.
- Si trois paires d’électrons sont partagées, la liaison est triple.
Pour qu’une liaison covalente se forme, trois conditions doivent être remplies :
- Les deux atomes doivent être des non-métaux.
- La différence d’électronégativité entre eux doit être inférieure à 1,7 (échelle de Pauling).
- Les atomes doivent respecter la règle du duet ou de l’octet afin d’être stables.
La liaison ionique
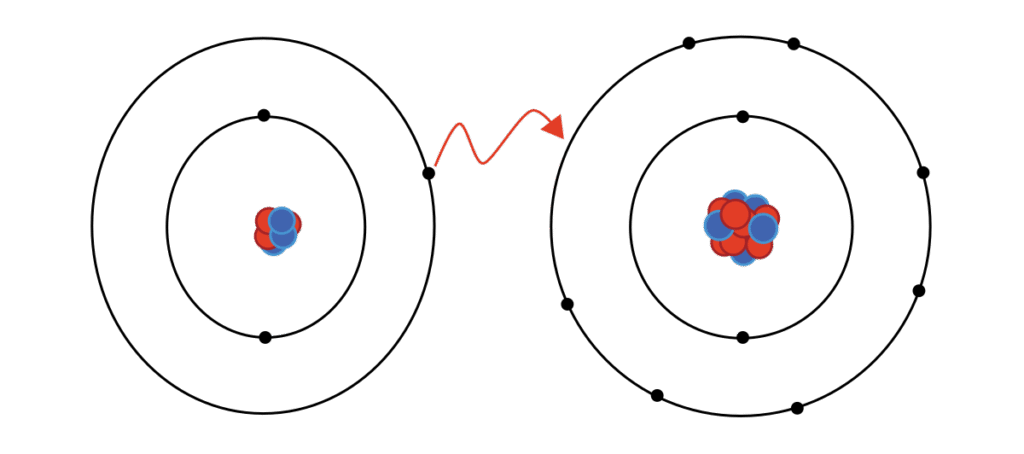
La liaison ionique est une liaison chimique qui se forme entre deux ions lorsque la différence d’électronégativité est importante, généralement entre un métal et un non-métal :
- Le métal perd un ou plusieurs électrons et devient un cation (ion positif).
- Le non-métal gagne ces électrons et devient un anion (ion négatif).
- Les ions obtenus respectent également la règle du duet ou de l’octet.
Propriétés de la liaison ionique
- La liaison ionique n’est ni orientée ni localisée.
- Dans un cristal ionique, les ions sont fixes et interagissent entre eux dans toutes les directions de l’espace.
- Un cristal ionique n’est pas constitué de molécules, mais d’un réseau ordonné d’ions.